横浜市立大学大学院医学研究科 薬理学教室の柴田 智博助教、徳留 健主任教授らの研究グループは、Cedars-Sinai Medical CenterのZakir Khan博士、Kenneth E. Bernstein博士らとの共同研究により、他家移植環境においても抗腫瘍免疫を活性化できる「抗原非依存型」のiPS細胞*1由来マクロファージ*2の樹立に成功しました。
アンジオテンシン変換酵素(ACE)*3は本来、血圧調節に関わる酵素として知られていますが、近年、免疫細胞の機能を強力に制御することが明らかになりつつあります。本研究では、Tet-On誘導システム*4を用いて、抗生物質ドキシサイクリン(Dox)の投与によってACE発現を制御できるヒトiPS細胞株を樹立しました。このiPS細胞を分化誘導して得られたACE高発現マクロファージ(ACE-iMac)は、ヒト化マウスモデル*5においてT細胞およびNK細胞の抗腫瘍活性を強力に増強することが明らかになりました。これらの結果から、本研究は、がん種に依存しない「抗原非依存型」の新しい細胞免疫療法の可能性を示すものです。
本研究成果は、国際学術誌「Signal Transduction and Targeted Therapy」に掲載されました(2026年4月13日公開)。
研究成果のポイント
研究背景
近年、免疫チェックポイント阻害薬やCAR-T細胞療法の登場により、がん免疫療法は大きく進展しました。しかし、固形がんでは治療抵抗性や再発が依然として大きな課題となっています。その要因の一つとして、腫瘍微小環境
*6において腫瘍関連マクロファージが免疫抑制的な性質(M2型)に偏り、抗腫瘍免疫を阻害していることが知られています。
このため、マクロファージを抗腫瘍型(M1型)へと再プログラムし、腫瘍局所の免疫環境を改善する新しい細胞療法の開発が期待されています。これまでの研究により、アンジオテンシン変換酵素(ACE)は好中球やマクロファージにおいて貪食能の増強や炎症性サイトカイン産生の促進に関与することが報告されています。
そこで本研究では、ACEを発現するiPS細胞を樹立し、そこからマクロファージへ分化誘導することで、宿主の抗腫瘍免疫を活性化できるiPS細胞由来マクロファージの開発を目指しました。
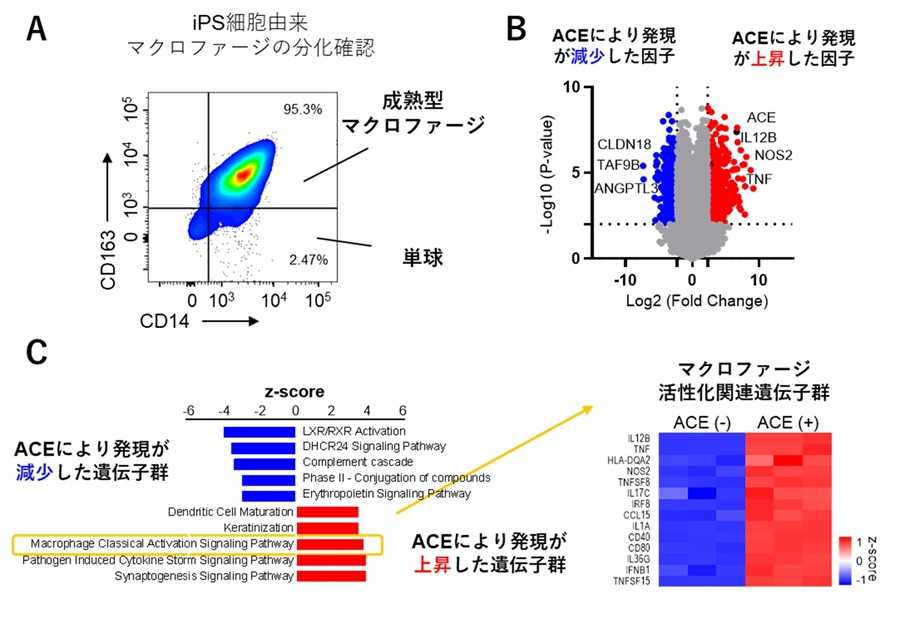
図1. ACEを発現させたiPS細胞由来マクロファージ(iMac)は、マクロファージ活性化や腫瘍内免疫細胞の活性化に関連する因子を高発現していた
A)iPS細胞から分化誘導した成熟型マクロファージの割合
B)ACE高発現iMacで発現が増加した因子と減少した因子
C)ACE高発現iMacで発現が上昇していた遺伝子群
研究内容
研究グループは、Tet-On誘導システムを用いて、抗生物質ドキシサイクリン(Dox)の投与によりACE発現を誘導できるヒトiPS細胞株を樹立しました。さらに、iPS細胞から効率よく成熟型マクロファージを得る分化プロトコールを確立しました(図1A)。この細胞株と分化系を用いて、以下の点を明らかにしました。
1. ACE発現によりマクロファージが強力ながん攻撃型へ転換
ACEを高発現させたACE-iMacでは、TNFαやIL-12などの炎症性サイトカインの産生が増加し、さらにがん細胞の細胞死を誘導する活性酸素(ROS)や一酸化窒素(NO)の産生が増強していました。これらの結果から、ACE-iMacは腫瘍促進型(M2型)ではなく、強い抗腫瘍活性を持つM1型の性質を示すことが分かりました。
また、網羅的遺伝子発現解析により、ACEを強制発現させたiMacでは、マクロファージ活性化や腫瘍内免疫細胞の活性化に関与する遺伝子群の発現が上昇していることが明らかになりました(図1B, C)。
2. 複数の固形がんモデルにおいて腫瘍増殖を強く抑制
ヌードマウス腫瘍移植モデル*7を用いた検討では、メラノーマ、トリプルネガティブ乳癌、多剤耐性頭頸部癌のいずれのモデルにおいても、ACE-iMac投与群で腫瘍体積が顕著に減少しました。
3. T細胞・NK細胞を活性化し、抗腫瘍免疫を増強
ヒト免疫系を導入したヒト化BLTマウスモデル*8においても、ACE-iMac治療は腫瘍増殖を有意に抑制しました。さらに、CD8陽性T細胞のIFN-γ産生及びNK細胞のパーフォリン産生が著明に増加しており、ACE-iMacによる抗腫瘍活性増強が確認されました。
本研究により、ACE-iMacは自らが腫瘍を攻撃するだけでなく、宿主の免疫細胞全体を活性化する「免疫ブースター」として機能することが明らかになりました。
今後の展開
今後は、今回行った腫瘍内投与でなく全身投与モデルでの検証や用量最適化と安全性評価を進めていきます。また、免疫チェックポイント阻害剤との併用効果についても検討を進め、最終的には臨床応用に向けた製造プロセスの確立を目指す予定です。
本研究で確立したACE-iMac療法は、固形がんに対する次世代免疫細胞療法として、臨床成績の向上に貢献する可能性があります。
論文情報
タイトル:Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth
著者:Tomohiro Shibata, Shabir Bhat, DuoYao Cao, Suguru Saito, Noor Khan, Ellen A. Bernstein, Takeshi Tokudome, Derick Okwan-Duodu, Warren G. Tourtellotte, Kenneth E. Bernstein, Zakir Khan
掲載雑誌:Signal Transduction and Targeted Therapy
DOI:
https://doi.org/10.1038/s41392-026-02650-3
用語説明
*1 iPS細胞(人工多能性幹細胞):体細胞に特定の遺伝子を導入することで作製される、多様な細胞へ分化できる能力を持つ細胞。再生医療や細胞治療への応用が期待されている。
*2マクロファージ:体内に侵入した病原体や異物を取り込み分解する免疫細胞の一種。腫瘍組織内では、がんを攻撃するタイプ(M1型)と、反対にがんの増殖を助けるタイプ(M2型)に分かれることが知られている。
*3アンジオテンシン変換酵素(ACE):血圧を調節するホルモン系(レニン–アンジオテンシン系)に関与する酵素。近年、免疫細胞の機能や炎症反応を調節する役割も持つことが明らかになっている。
*4 Tet-On誘導システム:特定の薬剤を加えることで遺伝子発現をオンにできる遺伝子制御技術。本研究では、抗生物質ドキシサイクリンを添加することでACEの発現を誘導した。
*5ヒト化マウスモデル:ヒトの免疫細胞や免疫系組織を移植して作製したマウスモデル。ヒトの免疫応答をマウスの体内で再現できるため、免疫療法の研究に広く用いられている。
*6腫瘍微小環境:腫瘍組織内に存在する免疫細胞、血管、線維芽細胞などから構成される腫瘍内の局所環境。がんの増殖や免疫応答に大きく影響する。
*7ヌードマウス腫瘍移植モデル:ヌードマウスは胸腺を持たずT細胞が欠損しているため、異種組織であるヒトがん細胞や組織を移植しても拒絶されにくく、ヒト由来のがん細胞の生着・増殖を評価するために利用される。
*8 BLTマウスモデル:骨髄(Bone marrow)、肝臓(Liver)、胸腺(Thymus)由来のヒト組織・細胞を移植して作製されるヒト化マウス。ヒトに近い免疫系を再構築できるモデルとして利用される。