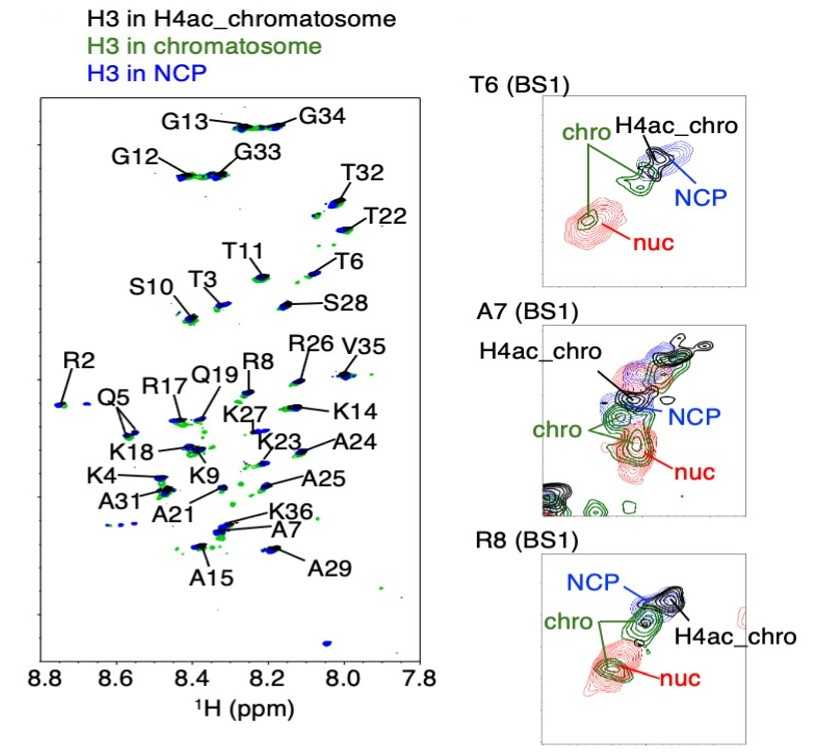
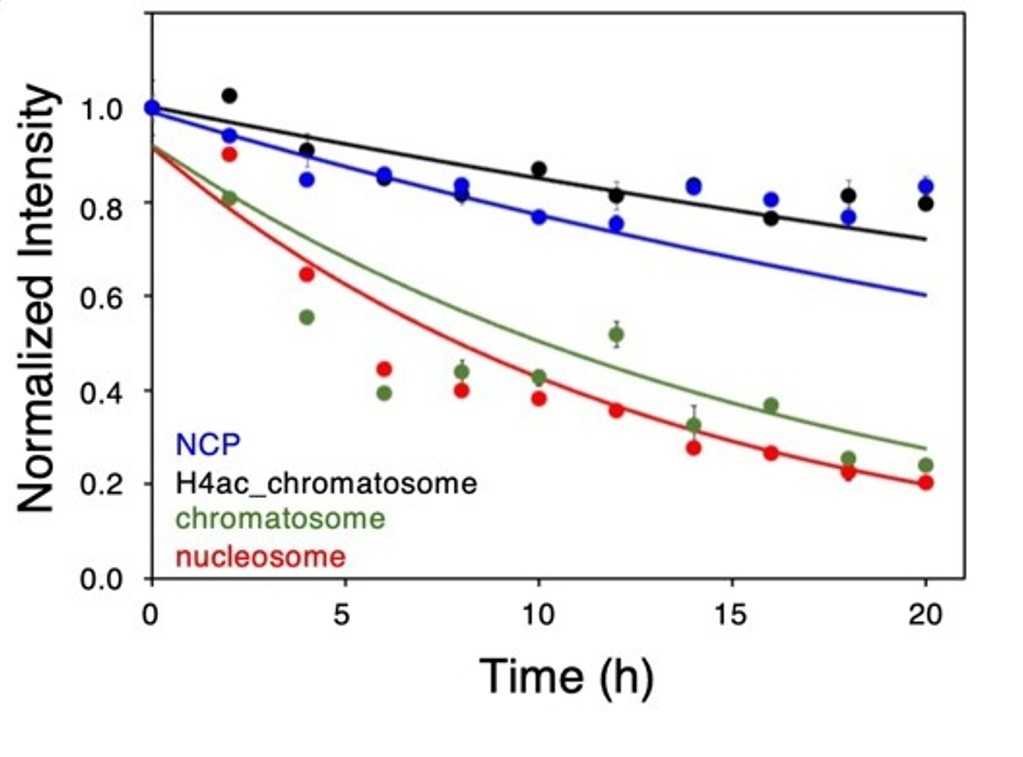
図5 H3N末テールのリシン14番のアセチル化反応の追跡
アセチル化酵素を加えた後で、NCP(青)、アセチル化クロマトソーム(黒)、クロマトソーム(緑)、ヌクレオソーム(赤)中のH3N末テールのリシン14番のNMRシグナルのアセチル化による強度変化を各時間でプロットした
今後の展開
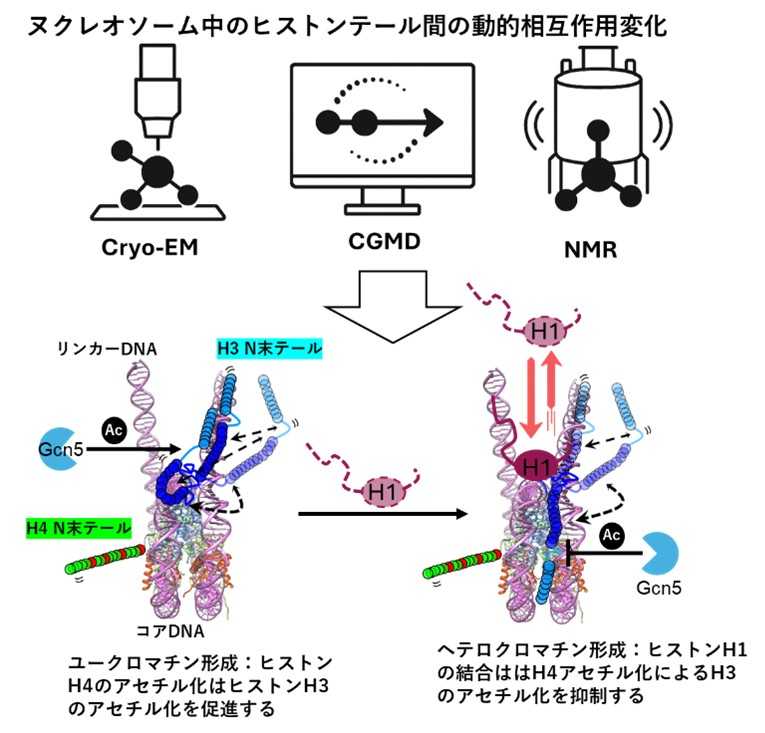
ヘテロクロマチンの形成は細胞の分化やがん化に於いて非常に重要で、ヘテロクロマチン構造の異常は個々の遺伝子の発現パターンを大きく変化させ、これが発がん過程、あるいは悪性化へ寄与しています。本研究で解明したユークロマチン形成とヘテロクロマチン形成に関与するリンカーヒストンH1の分子機構の解明は細胞分化や発がん過程の理解に役立つと考えられます。
研究費
本研究は、AMED創薬等ライフサイエンス研究支援基盤事業、文部科学省「先端研究基盤共用促進事業(共用プラットフォーム形成支援プログラム) NMR共用プラットフォーム」、JSPS科研費(基盤B)の一環で行われました。
論文情報
タイトル: Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics
著者:Ayako Furukawa, Kenta Echigoya, Samuel Blazquez, Masatoshi Wakamori, Hideaki Ohtomo, Yasuo Tsunaka, Takashi Umehara, Tsuyoshi Terakawa, Yoshimasa Takizawa, Hitoshi Kurumizaka and Yoshifumi Nishimura
掲載雑誌:Communications Biology
DOI:
https://doi.org/10.1038/s42003-026-09926-y
用語説明
*1 Cryo-EM(クライオ電子顕微鏡):解析試料を氷の中に分散し、電子顕微鏡で分散した各々の試料を個別に解析し、多数の電子顕微鏡像から3次元構造を再構築する。通常の電子顕微鏡では試料が真空中で干からびた構造になるが、Cryo-EMでは水溶液中の試料の3次元構造を氷の中に固めた状態で測定できるのでより機能構造が判る。最近の技術的な進歩により原子レベルでタンパク質やDNAとの複合体構造が解析できるようになった。
*2 CGMD(粗視化分子動力学計算):タンパク質中の全原子に基づく分子動力学計算に代わり、粗く原子集団で分子動力学計算を行う。
*3 NMR(核磁気共鳴):核スピンをもった原子核(1H、13C、15N)は強い磁場中で磁場の強度に応じて特異的にラジオ波(600MHz、800MHz、950MHz)を吸収し、タンパク質中の原子核の動的な情報を与える。ふらふらと揺らいでいるタンパク質部位の原子レベルでの同定が可能である。
参考文献
- Furukawa A, Wakamori M, Arimura Y, Ohtomo H, Tsunaka Y, Kurumizaka H, Umehara T,Nishimura Y. Acetylated histone H4 tail enhances histone H3 tail acetylation by altering their mutual dynamics in the nucleosome. Proc. Natl. Acad. Sci. U S A. 117, 19661-19663 (2020). doi: 10.1073/pnas.2010506117.
- Furukawa A, Wakamori M, Arimura Y, Ohtomo H, Tsunaka Y, Kurumizaka H, Umehara T,Nishimura Y.Characteristic H3 N-tail dynamics in the nucleosome core particle, nucleosome, and chromatosome. iScience. 2022; 25:103937. doi: 10.1016/j.isci.2022.103937.
- Tsunaka Y, Furukawa A,Nishimura Y. Histone tail network and modulation in a nucleosome. Curr Opin Struct Biol. 2022 75: 102436. doi: 10.1016/j.sbi.2022.102436.
- Okuda M., Tsunaka Y., Nishimura Y. Dynamic structures ofintrinsically disordered proteins related tothegeneral transcription factor TFIIH, nucleosomes, andhistone chaperones. Biophys Rev. 2022 14:1449-1472.doi: 10.1007/s12551-022-01014-9.
- Zhou, B., Feng, H., Kale, S., Fox, T., Khant, H., de Val, N., Ghirlando, R., Panchenko, A., and Bai, Y. Distinct Structures and Dynamics of Chromatosomes with Different Human Linker Histone Isoforms. Mol Cell 81, 166-182 (2021).